sexta-feira, 30 de setembro de 2011
Círculo-íris
Um fenômeno ótico formou um anel com as cores do arco-íris ao redor do Sol por volta do meio-dia desta sexta-feira (30) em Brasília. Segundo o Instituto Nacional de Meteorologia (Inmet), o fenômeno conhecido como halo é formado pelo reflexo do Sol em cristais de gelo.
“É um fenômeno meteorológico provocado por finíssimas luzes de cristais de gelo que ficam dentro das nuvens e são rebatidas pelo Sol”, disse o meteorologista do Inmet Manuel Rangel.
Segundo ele, os cristais de gelo são comuns nas nuvens mais finas e transparentes e o fenômeno não é incomum. “Não temos números sobre a frequência com que acontecem, mas é comum”, afirmou Rangel.
Segundo o meteorologista, a duração do halo é variável, podendo permanecer por até uma hora no céu.
Fonte: http://g1.globo.com/distrito-federal/noticia/2011/09/fenomeno-meteorologico-cria-arco-iris-em-torno-do-sol-em-brasilia.html
quinta-feira, 11 de agosto de 2011
quarta-feira, 18 de maio de 2011
quinta-feira, 31 de março de 2011
quarta-feira, 16 de março de 2011
1ª Avaliação de Ciências - Todas as notas já foram divulgadas
Para quem tirou uma boa nota parabéns. Para aqueles que não se saíram muito bem, corram atrás do prejuízo.
quinta-feira, 3 de março de 2011
Comentários sobre o experimento
Coloque um comentário sobre o experimento realizado na sala de Artes. Diga o que mais gostou e o que menos gostou. Coloque o seu nome e a sua turma antes do comentário.
quarta-feira, 2 de março de 2011
Aula 05 - Experimento 1 - O que são Materiais Homogêneos e Heterogêneos?
Procedimentos:
1º – cole um pedaço de fita em cada um dos tubos de ensaio, em seguida, numere os tubos plásticos de 1 a 9;
2º – Coloque água destilada nos tubos de 1 a 5 de moda a preencher metade do tubo;
3º – Tampe e separe o tubo 1, que ficará apenas com água. Nos tubos de 2 a 5, coloque:
Tubo 2: dez gotas de óleo e tampe;
Tubo 3: duas gotas de corante e tampe;
Tubo 4: dez gotas de removedor e tampe;
Tubo 5: duas palhetas de açúcar e tampe.
4º – Coloque óleo nos tubos de 6 a 9 de moda a preencher metade do tubo;
5º – Tampe e separe o tubo 6, que ficará apenas com óleo. Nos tubos de 7 a 9, coloque:
Tubo 7: duas gotas de corante e tampe;
Tubo 8: dez gotas de removedor e tampe;
Tubo 9: duas palhetas de açúcar e tampe.
Agite os três tubos.
Discussão do experimento
Obs.: As questões deverão ser respondidas em grupo
1 – Preencha a tabela DISSOLVE, SIM OU NÃO?
2 – Os materiais presentes nos tubos 2 e 3 se misturaram?
3 – O corante se dissolveu na água (tubo 3), mas será que ele se dissolveu no óleo (tubo 7)? Justifique através das suas observações.
1º – cole um pedaço de fita em cada um dos tubos de ensaio, em seguida, numere os tubos plásticos de 1 a 9;
2º – Coloque água destilada nos tubos de 1 a 5 de moda a preencher metade do tubo;
3º – Tampe e separe o tubo 1, que ficará apenas com água. Nos tubos de 2 a 5, coloque:
Tubo 2: dez gotas de óleo e tampe;
Tubo 3: duas gotas de corante e tampe;
Tubo 4: dez gotas de removedor e tampe;
Tubo 5: duas palhetas de açúcar e tampe.
4º – Coloque óleo nos tubos de 6 a 9 de moda a preencher metade do tubo;
5º – Tampe e separe o tubo 6, que ficará apenas com óleo. Nos tubos de 7 a 9, coloque:
Tubo 7: duas gotas de corante e tampe;
Tubo 8: dez gotas de removedor e tampe;
Tubo 9: duas palhetas de açúcar e tampe.
Agite os três tubos.
Discussão do experimento
Obs.: As questões deverão ser respondidas em grupo
1 – Preencha a tabela DISSOLVE, SIM OU NÃO?
2 – Os materiais presentes nos tubos 2 e 3 se misturaram?
3 – O corante se dissolveu na água (tubo 3), mas será que ele se dissolveu no óleo (tubo 7)? Justifique através das suas observações.
Aula 04
Temperatura de Fusão e Ebulição
Atividade 04
1) Sabendo que a região do Rodeador próximo de Brazlândia está a 1342 m e que a cidade de Ceilândia está a 1200 m, ambas acima do nível do mar. Diga em qual cidade a água entrará em ebulição primeiro. Justifique.
2) Um cientista descobriu a substância X e identificou que a sua temperatura de ebulição é 120 ºC e a sua temperatura de fusão é -2 º C. Indique o seu estado físico nas seguintes temperaturas:
a) -5 º C
b) 80 º C
c) 150 º C
d) 119 º C
e) -1 º C
f) 120 º C
3) Diga o que é pressão atmosférica e como ela se relaciona com a altitude e com a temperatura de ebulição das substâncias.
1342 m
Atividade 04
1) Sabendo que a região do Rodeador próximo de Brazlândia está a 1342 m e que a cidade de Ceilândia está a 1200 m, ambas acima do nível do mar. Diga em qual cidade a água entrará em ebulição primeiro. Justifique.
2) Um cientista descobriu a substância X e identificou que a sua temperatura de ebulição é 120 ºC e a sua temperatura de fusão é -2 º C. Indique o seu estado físico nas seguintes temperaturas:
a) -5 º C
b) 80 º C
c) 150 º C
d) 119 º C
e) -1 º C
f) 120 º C
3) Diga o que é pressão atmosférica e como ela se relaciona com a altitude e com a temperatura de ebulição das substâncias.
1342 m
quarta-feira, 23 de fevereiro de 2011
Aula 03
Propriedades da Matéria
Transformações Químicas: são as transformações que envolvem mudança na constituição das substâncias. Por exemplo, lixo se transformando em adubo.
Transformações Físicas: são as transformações que não envolvem mudança na constituição das substâncias. Por exemplo, um cubo de gelo derretendo.
Estados Físicos da Matéria
Estado Sólido: no estado sólido a matéria tem forma e volume definidos. Exemplo: ferro, ouro, alumínio, diamante, cloreto de sódio e outros.
Estado Líquido: a matéria não tem forma própria, mas o volume permanece constante, exemplo: água, acetona, gasolina, álcool e outros.
Estado Gasoso: a matéria não tem forma nem volume definidos, exemplo: oxigênio, nitrogênio, gás carbônico e outros.
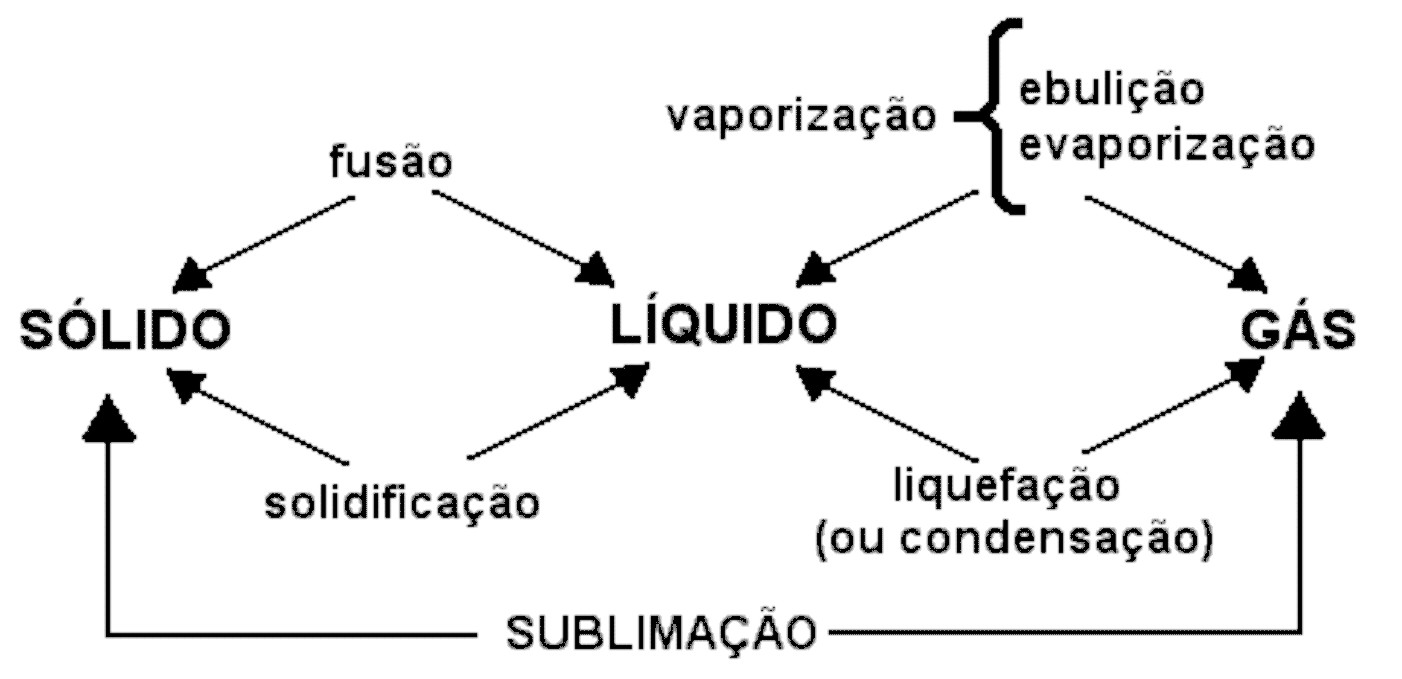
As Mudanças de Estados Físicos
Fusão: é a transformação de uma substância do estado sólido para o estado líquido.
Solidificação: é a transformação de uma substância do estado líquido para o estado sólido.
Condensação: é a transformação de uma substância do estado gasoso para o estado líquido.
Sublimação: é a transformação de uma substância do estado sólido direto para o estado gasoso.
Vaporização: é a transformação de uma substância do estado líquido para o estado gasoso Pode ocorrer por meio da ebulição e da evaporação.
Ebulição: Ocorre quando fornecemos calor a um líquido
Evaporação: Ocorre de maneira lenta, espontânea e depende das condições ambientais.
Atividade 03
1)Complete a tabela abaixo com os termos: definido ou indefinido.
2) Qual a diferença entre ebulição e evaporação? Cite exemplos de cada uma delas.
3) Cite exemplos de substâncias no estado sólido, líquido e gasoso.
4) Diferencie transformações físicas de transformações químicas. Cite exemplos de cada uma delas.
Transformações Químicas: são as transformações que envolvem mudança na constituição das substâncias. Por exemplo, lixo se transformando em adubo.
Transformações Físicas: são as transformações que não envolvem mudança na constituição das substâncias. Por exemplo, um cubo de gelo derretendo.
Estados Físicos da Matéria
Estado Sólido: no estado sólido a matéria tem forma e volume definidos. Exemplo: ferro, ouro, alumínio, diamante, cloreto de sódio e outros.
Estado Líquido: a matéria não tem forma própria, mas o volume permanece constante, exemplo: água, acetona, gasolina, álcool e outros.
Estado Gasoso: a matéria não tem forma nem volume definidos, exemplo: oxigênio, nitrogênio, gás carbônico e outros.
As Mudanças de Estados Físicos
Fusão: é a transformação de uma substância do estado sólido para o estado líquido.
Solidificação: é a transformação de uma substância do estado líquido para o estado sólido.
Condensação: é a transformação de uma substância do estado gasoso para o estado líquido.
Sublimação: é a transformação de uma substância do estado sólido direto para o estado gasoso.
Vaporização: é a transformação de uma substância do estado líquido para o estado gasoso Pode ocorrer por meio da ebulição e da evaporação.
Ebulição: Ocorre quando fornecemos calor a um líquido
Evaporação: Ocorre de maneira lenta, espontânea e depende das condições ambientais.
Atividade 03
1)Complete a tabela abaixo com os termos: definido ou indefinido.
| Estado Físico | Forma | Volume |
| Sólido | ||
| Líquido | ||
| Gasoso |
2) Qual a diferença entre ebulição e evaporação? Cite exemplos de cada uma delas.
3) Cite exemplos de substâncias no estado sólido, líquido e gasoso.
4) Diferencie transformações físicas de transformações químicas. Cite exemplos de cada uma delas.
terça-feira, 22 de fevereiro de 2011
Aula 02
Matéria e Energia
Atividade 02
1)Diferencie os itens abaixo em matéria ou energia. Justifique suas respostas:
a) calor
b) gelo
c) vapor de água
d) cinzas
e) luz
f) eletricidade
2) um planeta pode ser considerado um corpo? Justifique.
3) Explique o que é massa e como podemos medi-la?
4) Qual a diferença entre massa e volume?
Atividade 02
1)Diferencie os itens abaixo em matéria ou energia. Justifique suas respostas:
a) calor
b) gelo
c) vapor de água
d) cinzas
e) luz
f) eletricidade
2) um planeta pode ser considerado um corpo? Justifique.
3) Explique o que é massa e como podemos medi-la?
4) Qual a diferença entre massa e volume?
Aula 01
Nessa aula foi feita a leitura dos textos disponíveis nos links abaixo:
Texto 01: Quando Crescer vou ser um Químico. Clique aqui para ler o texto
Texto 02: Quando Crescer vou ser um Físico. Clique aqui para ler o texto
Atividade 01
1 - O que é ser um Físico/Químico?
2 - Qual a importância do Físico/Químico para a sociedade?
3 - O que você faria se fosse um Físico/Químico?
4 - Elabore três questões com respostas sobre o texto.
Texto 01: Quando Crescer vou ser um Químico. Clique aqui para ler o texto
Texto 02: Quando Crescer vou ser um Físico. Clique aqui para ler o texto
Atividade 01
1 - O que é ser um Físico/Químico?
2 - Qual a importância do Físico/Químico para a sociedade?
3 - O que você faria se fosse um Físico/Químico?
4 - Elabore três questões com respostas sobre o texto.
sexta-feira, 28 de janeiro de 2011
Livro de Experimentos
Gostariamos de informar que já se encontra disponível, no portal do Ano Internacional da Quimica 2011, o projeto " A Química perto de você: experimentos de baixo custo para a sala de aula do ensino fundamental e médio".
Para esta primeira edição, foram compilados preferencialmente os experimentos que não envolvessem solventes com alta volatilidade, a necessidade de aquecimento mais efetivo e que praticamente não envolvessem a geração de resíduos, visto que o foco era gerar material para apoio à sala de aula.

Deste modo, agradecemos a colaboração de todos e informamos que os experimentos que não constam deste material serão inseridos numa segunda edição, que será disponibilizada ainda no ano de 2011 e que, como a primeira, terá seu ISBN junto à biblioteca nacional. Aproveitamos para esclarecer que este material será distribuido as escolas públicas brasileiras pelo MEC, numa promessa de 100 mil exemplares, no formato de DVD, e que estará disponível brevemente no portal do professor, na página do MEC.
Esta compilação de experimentos está acompanhada, no DVD, de 7 e-books sobre a Química no Cotidiano e da coleção da Química Nova na Escola, com mecanismo de busca.
Um ótimo Ano Internacional da Quimica a todos,
Claudia M. Rezende
Tesoureira da Sociedade Brasileira de Química
Instituto de Química
Universidade Federal do Rio de Janeiro
(21) 2562-7370/ 7121
Para fazer o DOWNLOAD do arquivo clique Download (tamanho ~1.5MB em PDF)
Gostariamos de informar que já se encontra disponível, no portal do Ano Internacional da Quimica 2011, o projeto " A Química perto de você: experimentos de baixo custo para a sala de aula do ensino fundamental e médio".
Para esta primeira edição, foram compilados preferencialmente os experimentos que não envolvessem solventes com alta volatilidade, a necessidade de aquecimento mais efetivo e que praticamente não envolvessem a geração de resíduos, visto que o foco era gerar material para apoio à sala de aula.

Deste modo, agradecemos a colaboração de todos e informamos que os experimentos que não constam deste material serão inseridos numa segunda edição, que será disponibilizada ainda no ano de 2011 e que, como a primeira, terá seu ISBN junto à biblioteca nacional. Aproveitamos para esclarecer que este material será distribuido as escolas públicas brasileiras pelo MEC, numa promessa de 100 mil exemplares, no formato de DVD, e que estará disponível brevemente no portal do professor, na página do MEC.
Esta compilação de experimentos está acompanhada, no DVD, de 7 e-books sobre a Química no Cotidiano e da coleção da Química Nova na Escola, com mecanismo de busca.
Um ótimo Ano Internacional da Quimica a todos,
Claudia M. Rezende
Tesoureira da Sociedade Brasileira de Química
Instituto de Química
Universidade Federal do Rio de Janeiro
(21) 2562-7370/ 7121
Para fazer o DOWNLOAD do arquivo clique Download (tamanho ~1.5MB em PDF)
Assinar:
Comentários (Atom)